Elucidación de estructuras con absorción IR
- 8 oct 2019
- 5 Min. de lectura
Fundamentos teóricos y metodológicos

Espectroscopía infrarroja
La región infrarroja del espectro incluye la radiación con números de onda comprendidos entre los 12.800 y los 10 cm-1, lo que corresponde a longitudes de onda de 0,78 a 1000 mm. Tanto desde el punto de vista de las aplicaciones como de los instrumentos, es conveniente subdividir el espectro infrarrojo en tres regiones denominadas infrarrojo cercano (λ entre 0,78 y 2,5 μm), medio (λ entre 2,5 y 50 μm) y lejano (λ entre 50 y 1000 μm). Hasta la fecha, la gran mayoría de las aplicaciones analíticas se han restringido al uso de una parte de la región del infrarrojo medio comprendida entre los 4000 y los 400 (1/cm) (de 2,5 a 25 μm). Sin embargo, en la literatura analítica actual, se van encontrando un número creciente de aplicaciones de la espectroscopia infrarroja cercana y lejana.
en muchos casos, el espectro infrarrojo medio de un compuesto orgánico proporciona una huella única, con unas características que se distinguen fácilmente de los modelos de absorción del resto de compuestos; sólo los isómeros ópticos absorben exactamente de la misma forma

La espectroscopía infrarroja tiene una gran aplicación en el análisis cualitativo y cuantitativo. Su principal utilización ha sido la identificación de compuestos orgánicos, que por lo general presentan espectros complejos en el infrarrojo medio con numerosos máximos y mínimos que resultan útiles al efectuar comparaciones. En muchos casos, el espectro infrarrojo medio de un compuesto orgánico proporciona una huella única, con unas características que se distinguen fácilmente de los modelos de absorción del resto de compuestos; sólo los isómeros ópticos absorben exactamente de la misma forma.
Interacción de la radiación infrarroja con las moléculas orgánicas

La radiación infrarroja no es suficientemente energética como para producir las transiciones electrónicas que se dan cuando se trata de las radiaciones ultravioleta y visible. La absorción de radiación infrarroja se limita así en gran parte a especies moleculares para las cuales existen pequeñas diferencias de energía entre los distintos estados vibracionales y rotacionales.
Moléculas activas en el IR

Para absorber radiación infrarroja, una molécula debe experimentar un cambio neto en el momento dipolar como consecuencia de su movimiento de vibración o de rotación. Sólo en estas circunstancias, el campo eléctrico alternante de la radiación puede interaccionar con la molécula, y causar así cambios en la amplitud de alguno de sus movimientos. El momento dipolar está determinado por la magnitud de la diferencia de carga y por la distancia entre ambos centros de carga. Cuando se trata de especies homonucleares como el oxígeno, nitrógeno o cloro gaseosos, el momento dipolar no se altera durante la vibración o la rotación y, en consecuencia, este tipo de compuestos no absorben en el infrarrojo.

Un fotón de la zona del IR será absorbido por una molécula si, además, es resonante con la frecuencia de vibración natural de la molécula.

Pueden distinguirse dos tipos básicos de vibraciones: de tensión y de flexión. Una vibración de tensión supone un cambio continuo en la distancia interatómica a lo largo del eje del enlace entre dos átomos. Las vibraciones de flexión se caracterizan por un cambio en el ángulo entre dos enlaces y son de cuatro tipos: de tijereteo, de balanceo, de aleteo y de torsión.
La absorción de fotones del IR por parte de moléculas orgánicas depende de los tipos atómicos implicados en el enlace (cromóforos), del entorno químico del enlace (auxócromos) y de la concentración de enlaces presentes (ley de Lambert y Beer).
Espectros moleculares en el infrarrojo

Un espectro infrarrojo es característico, y, a diferencia de lo que sucede en la mayoría de los espectros en las regiones ultravioleta y visible, se observan una gran cantidad de máximos y mínimos. En ellos, la ordenada corresponde a una escala lineal de % de transmitancia y la abscisa mide linealmente los números de onda en unidades de 1/cm.

Como se grafica el %T, los picos de absorción de fotones se ven como un mínimo en lugar de un máximo, como ocurre cuando se grafica Absorbancia. Nótese que los valores de número de onda aumenta hacia la izquierda. Por lo tanto, la energía, frecuencia aumentan hacia la izquierda, mientras que la longitud de onda lo hace hacia la derecha.
El espectro IR se divide en dos zonas según su aplicación en la identificación de compuestos orgánicos: La región de frecuencias de grupo, que abarca la radiación comprendida desde los 4000 (1/cm) a los 1500 (1/cm) aproximadamente, y la región de huella dactilar, que abarca la radiación comprendida desde los 1500 (1/cm) a los 500 (1/cm).
La región de frecuencias de grupo corresponde a la región de identificación de los grupos funcionales.
La región de huella dactilar es muy útil para diferenciar isómeros, debido a que pequeñas diferencias en la estructura y la constitución de una molécula provocan cambios significativos en el aspecto y la distribución de los picos en esta región.
Principios de la absorción de fotones en el IR por parte de moléculas orgánicas
Los grupos funcionales absorben en zonas diferentes del espectro según determinados principios básicos, que se relacionan con el modelo de enlace químico como dos esferas de una determinada masa unidas por un resorte:
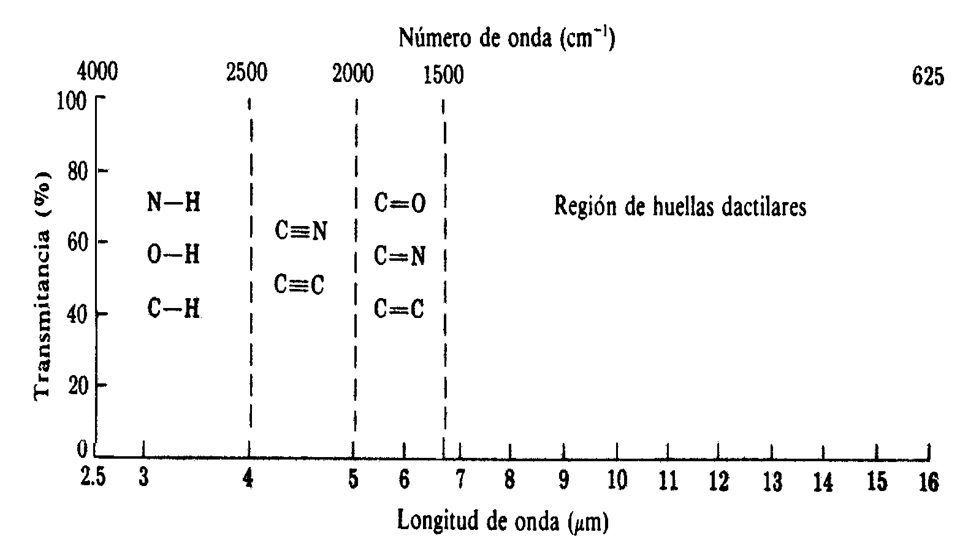
Los enlaces cortos y fuertes necesitan mayor energía para estirarlos: los enlaces triples absorben fotones de mayor energía que los enlaces dobles, los cuales, a su vez, absorben fotones de mayor energía que los enlaces simples.
Los resortes que unen masas pequeñas (átomos livianos) vibran más rápido que los más pesados, por lo cual necesitan fotones de mayor energía: los enlaces con H (CH, OH, NH), absorben a mayor frecuencia que los enlaces de átomos más pesados.

Espectrofotómetro de Infrarrojo

Este instrumento está basado en el principio del interferómetro de Michelson, que funciona del siguiente modo: la radiación primero golpea a un divisor o separador que escinde el haz de la luz en dos partes iguales (espejo semirreflejante). Estos dos haces de luz interfieren en el divisor después en su viaje de vuelta cuando son reflejados sobre otros dos espejos. Uno dispuesto frente a la trayectoria del haz original (espejo móvil 1) y el otro perpendicular (espejo fijo 2). En esta trayectoria se dispone la muestra, luego el monocromador y a continuación el detector IR. La intensidad resultante de la superposición de los dos haces es medida como función del desfase (s) del espejo móvil en su desplazamiento respecto la posición intermedia.
Tratamiento de la muestra para medir en el IR
El estado de agregación de la muestra afecta a la determinación, ya que ello, a su vez, determina el grado de movimientos rotacionales (los cuales es deseable evitar) y de interacciones intermoleculares. Las muestras usadas pueden estar en estado sólido o líquido. Las muestras gaseosas tienen abundancia en movimientos rotacionales y escasa interacción intermolecular. Por su parte, las muestras líquidas poseen alguna superposición de movimientos rotacionales y abundancia de interacciones intermoleculares, mientras que las sólidas sólo presentan movimientos vibracionales y variaciones en el estado cristalino.
Las muestras líquidas pueden ser prensadas entre dos planchas de una sal de alta pureza (como el cloruro de sodio). Estas placas deben ser transparentes a la luz infrarroja para no introducir ninguna línea en el espectro de la muestra. Las placas obviamente son solubles en agua, por lo que la muestra, los reactivos de lavado y el medio deben ser anhidros.

Las muestras sólidas se preparan mezclando una cierta cantidad de muestra con una sal altamente purificada (por lo general bromuro de potasio), en una proporción aproximada de 1/10. Esta mezcla se tritura y se prensa con el fin de formar una pastilla por la que pueda pasar la luz.
Videos sugeridos
Comentarios