Análisis de nitrógeno en proteína
- 17 oct 2019
- 1 Min. de lectura
Determinación por espectrofotometría de absorción molecular en el UV-Visible

Problema
El amoníaco puede determinarse espectrofotométricamente por reacción con fenol en presencia de hipoclorito:
Una muestra de 4,37 mg de proteína fue químicamente desnaturalizada para convertir su nitrógeno en amoníaco. Después de este tratamiento, el volumen de la muestra fue de 100 mL. Luego, 10,0 mL de esta solución se colocaron en un frasco volumétrico de 50 mL y se trataron con 5 mL de solución de fenol más 2 mL de solución de hipoclorito de sodio (NaClO).
La muestra se diluyó a 50 mL y, después de 30 minutos, se obtuvo a 625 nm el valor de absorbancia en una celda de 1,00 cm de espesor.
Como referencia se preparó una solución estándar con 0,0100 g de cloruro de amonio (PM = 53,49) disueltos en 1,000 L con agua. En un frasco volumétrico de 50,0 mL se colocaron 10,0 mL de la solución estándar y se trataron de la misma forma que la muestra desconocida. Los datos se muestran en la siguiente tabla.
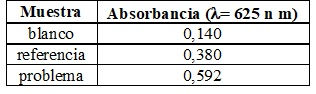
Calcular la absortividad molar del producto azul y el % en peso de Nitrógeno en la proteína.
Comentarios